Fermentas
Šis straipsnis apie katalizatorių. Apie įmonę skaitykite straipsnyje Fermentas (įmonė).

Fermentas – baltyminis katalizatorius, paspartinantis organizme vykstančias chemines reakcijas tūkstančius kartų. Be fermentų šios reakcijos nevyktų arba vyktų labai lėtai, ir organizmai negalėtų egzistuoti. Fermentai naudojami kaip vaistiniai preparatai, kaip reagentai ar biocheminiai rodikliai diagnozei nustatyti. Šiuo metu ištirta daugiau kaip 3000 fermentų.[1]
Veikimo mechanizmas
[redaguoti | redaguoti vikitekstą]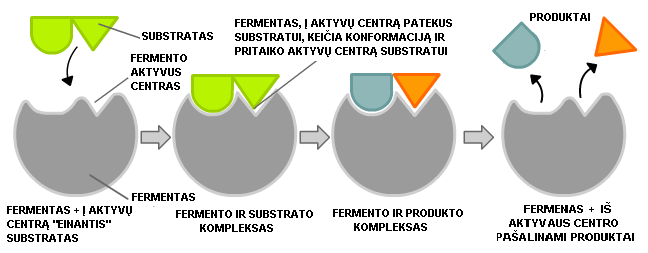

Fermentas sąveikauja su substratu (ar substratais), pakeičia jo struktūrą, t. y., substratą verčia į produktą. Fermentinė reakcija vyksta tik tam tikroje fermento dalyje – aktyviajame centre, kurį sudaro, formuojantis tretinei baltymo struktūrai iš skirtingų baltymo molekulės vietų, suartėjusios amino rūgščių liekanos. Aktyvus centras turi substrato jungimo ir katalizinę sritis.
Yra pasiūlyti modeliai, aiškinantys, kaip fermentas savo aktyviajame centre sąveikauja su substrato molekule. „Spynos ir rakto“ modelis teigia, kad fermento ir jo substrato sąveika galima tik tuomet, kai substratas atitinka aktyvų centrą taip, kaip raktas spyną. Kitas biokatalizės mechanizmus aiškinantis modelis teigia, kad sąveikaujant substratui su aktyviuoju centru, gali keistis arba substrato, arba aktyviojo centro, arba abiejų erdvinės struktūros taip, kad būtų palankiausia struktūra substrato molekulę pakreipti katalizinių grupių link. Prie fermento baltyminės dalies (apofermento), kad jis galėtų atlikti savo funkcijas, aktyvajame centre prijungiama nebaltyminė dalis – kofaktorius. Susijungę apofermentas ir kofermentas sudaro funkcionalią struktūrą, vadinamą holofermentu.
Klasifikacija
[redaguoti | redaguoti vikitekstą]Fermentai pagal katalizuojamos reakcijos tipą skirstomi į 6 klases (lentelė). Literatūroje dažnai sutinkami darbiniai (trivialieji) fermentų pavadinimai, kurie sudaromi prie substrato ar katalizuojamos reakcijos pavadinimo pridedant galūnę -azė (alkoholdehidrogenazė, karboksipeptidazė)
| Klasė | Katalizuojama reakcija | Reakcijos pavyzdys | Poklasiai |
|---|---|---|---|
| 1 Oksidoreduktazės |
Katalizuoja oksidacijos – redukcijos procesus. Iš oksiduojamo substrato paimtus elektronus perduoda redukuojamam | AH + B → A + BH (redukuota forma) A + O → AO (oksiduota forma) |
Dehidrogenazės, peroksidazės ir reduktazės ir kt. |
| 2 Transferazės |
Katalizuoja funkcinių grupių (metil-, acil-, amino- ar fosfatinės grupių) pernašą nuo vienos molekulės prie kitos arba nuo vienos molekulės dalies į kitą tos pačios molekulės dalį. | AB + C → A + BC | Aciltransferazės, metiltrasferazės, kinazės ir kt. |
| 3 Hidrolazės |
Katalizuoja cheminių ryšių (C-O, C-N, C-S) skaidymą dalyvaujant vandeniui. | AB + H2O → AOH + BH | Esterazės ir kt. |
| 4 Liazės |
Nedalyvaujant vandeniui skaido ryšius tarp substrato atomų (C-C, C-N, C-O ar C-S), gali sudaryti naujus dvigubus ryšius suskaidyto ryšio vietoje. | RCOCOOH → RCOH + CO2 | Dekarboksilazės, dehidratazės ir kt. |
| 5 Izomerazės |
Katalizuoja tos pačios molekulės vidumolekulinį persigrupavimą. | AB → BA | Mutazės, racemazės ir kt. |
| 6 Ligazės |
Naudodami ATP hidrolizės metu išsiskiriančią energiją, katalizuoja C-O, C-S, C-N ar C-C kovalentinių ryšių susidarymą. | X + Y+ ATP → XY + ADP + Pi | Sintetazė |
Žmogaus organizme yra aptikta daugiau nei 5 tūkst. 22 skirtingų tipų fermentų, kurių daugelis gaminama kasoje. Trys pagrindiniai virškinimo fermentai yra amilazė, lipazė ir proteazė, kurie atitinkamai skaido angliavandenius, riebalus ir baltymus.
Savybės
[redaguoti | redaguoti vikitekstą]
Fermentai, kaip visi katalizatoriai, reakcijos metu nėra nei sunaudojami, nei pagaminami. Jie nekeičia reakcijos pusiausvyros, o tik padidina reakcijos greitį. Tik fermentams būdinga tai, kad jie sąveikauja griežtai tik su tam tikrais substratais, yra stereospecifiški. Jie yra jautrūs temperatūros, terpės pH pokyčiams.
Fermentų aktyvumas yra reguliuojamas modifikuojant (pvz.: fosforilinant, metilinant), veikiant inhibitoriais (bet kuri cheminė medžiaga, mažinanti reakcijos greitį) ar aktyvatoriais, keičiant fermento kiekį (baltymai organizme po tam tikro laiko degraduojami; sintetinami tik esant induktoriui) ir kt.
Fermentas yra aktyvus tik tam tikroje temperatūroje. Temperatūrai didėjant fermentas ima denatūruoti ir nebeatlieka savo funkcijos. Kylant temperatūrai iki tam tikros ribos, reakcijos greitis didėja, nes didėja galimybė susidurti substrato ir fermento molekulėms ir jų kinetinė energija. Reakcijos greitis priklauso nuo aktyvių fermentų kiekio. Jei yra pakankamai substrato ir tam tikra temperatūra ir pH tai reakcijos greitis bus proporcingas fermentų koncentracijai.
Šaltiniai
[redaguoti | redaguoti vikitekstą]- ↑ KRYLOVA Valentina, RINKEVIČIENĖ Elvyra. Cheminiai elementai biologinėse sistemose: mokomoji knyga . Vilnius: Vilniaus pedagoginio universiteto leidykla, 2008, 56 p. ISBN 978-9955-20-311-7.